Bioelemento
Los bioelementos o elementos biogénicos son los elementos químicos, presentes en seres vivos.
La materia viva está constituida por unos 70 elementos, la práctica
totalidad de los elementos estables que hay en la Tierra, excepto los gases nobles.1 No obstante, alrededor del 99% de la masa de la mayoría de las células está constituida por cuatro elementos, carbono (C), hidrógeno (H), oxígeno (O) y nitrógeno (N), que son mucho más abundantes en la materia viva que en la corteza terrestre.2
Tipos de bioelementos
Según su intervención en la constitución de las biomoléculas, los bioelementos se clasifican en primarios y secundarios.
Bioelementos primarios
Los bioelementos primarios son los elementos indispensables para formar las biomoléculas orgánicas (glúcidos, lípidos, proteínas y ácidos nucleicos);
constituyen el 96% de la materia viva seca. Son el carbono, el
hidrógeno, el oxígeno, el nitrógeno, el fósforo y el azufre (C, H, O, N,
P, S, respectivamente).
- Carbono: tiene la capacidad de formar largas cadenas carbono-carbono (macromoléculas) mediante enlaces simples (-CH2-CH2) o dobles (-CH=CH-), así como estructuras cíclicas. Pueden incorporar una gran variedad de radicales (=O, -OH, -NH2, -SH, PO43-), lo que da lugar a una variedad enorme de moléculas distintas. Los enlaces que forma son lo suficientemente fuertes como para formar compuestos estables, y a la vez son susceptibles de romperse sin excesiva dificultad. Por esto, la vida está constituida por carbono y no por silicio, un átomo con la configuración electrónica de su capa de valencia igual a la del carbono. El hecho es que las cadenas silicio-silicio no son estables y las cadenas de silicio y oxígeno son prácticamente inalterables, y mientras el dióxido de carbono, CO2, es un gas soluble en agua, su equivalente en el silicio, SiO2, es un cristal sólido, muy duro e insoluble (cuarzo).
- Hidrógeno: además de ser uno de los componentes de la molécula de agua, indispensable para la vida y muy abundante en los seres vivos, forma parte de los esqueletos de carbono de las moléculas orgánicas. Puede enlazarse con cualquier bioelemento.

Ácido oleico, una cadena de 18 átomos de carbono (bolas negras); las bolas blancas son átomos de hidrógeno y las rojas àtomos de oxígeno.
- Oxígeno: es un elemento muy electronegativo que permite la obtención de energía mediante la respiración aeróbica. Además, forma enlaces polares con el hidrógeno, dando lugar a radicales polares solubles en agua (-OH, -CHO, -COOH).
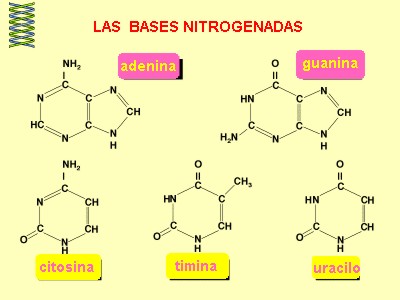
- Nitrógeno: principalmente como grupo amino (-NH2) presente en las proteínas ya que forma parte de todos los aminoácidos. También se halla en las bases nitrogenadas de los ácidos nucleicos. Prácticamente todo el nitrógeno es incorporado al mundo vivo como ion nitrato, por las plantas. El gas nitrógeno solo es aprovechado por algunas bacterias del suelo y algunas cianobacterias.
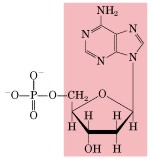
- Fósforo. Se halla principalmente como grupo fosfato (PO43-) formando parte de los nucleótidos. Forma enlaces ricos en energía que permiten su fácil intercambio (ATP).
- Azufre. Se encuentra sobre todo como radical sulfhidrilo (-SH) formando parte de muchas proteínas, donde crean enlaces disulfuro esenciales para la estabilidad de la estructura terciaria y cuaternaria. También se halla en el coenzima A, esencial para diversas rutas metabólicas universales, como el ciclo de Krebs.
Bioelementos secundarios
Los bioelementos secundarios se encuentran en menor proporción en
todos los seres vivos, en forma iónica, en proporción de 4,5 %. Se
clasifican en dos grupos: los indispensables y los variables.
Bioelementos secundarios indispensables. Están presentes en
todos los seres vivos. Los más abundantes son el sodio, el potasio, el
magnesio y el calcio. Los iones sodio, potasio y cloruro intervienen en
el mantenimiento del grado de salinidad del medio interno y en el
equilibrio de cargas a ambos lados de la membrana. Los iones sodio y
potasio son fundamentales en la transmisión del impulso nervioso; el
calcio en forma de carbonato da lugar a caparazones de moluscos y al
esqueleto de muchos animales. El ion calcio actúa en muchas reacciones,
como los mecanismos de la contracción muscular, la permeabilidad de las
membranas, etc. El magnesio es un componente de la clorofila y de muchas enzimas. Interviene en la síntesis y la degradación del ATP, en la replicación del ADN y en su estabilización, etc.
Bioelementos secundarios variables. Están presentes en algunos seres vivos.
Clasificación de los bioelementos
Los bioelementos también se clasifican en mayoritarios, traza y ultratraza.
Bioelementos mayoritarios. Se presentan en cantidades superiores al 0,1% del peso del organismo. Oxígeno (O), carbono (C), hidrógeno (H), nitrógeno (N), calcio (Ca), fósforo (P), azufre (S), cloro (Cl) y sodio (Na).
Bioelementos traza. Están presentes en una proporción comprendida entre el 0,1% y el 0,0001% del peso de un ser vivo. Entre otros se incluye silicio (Si), magnesio (Mg) y cobre (Cu).
Bioelementos ultratraza. Se presentan en cantidades inferiores al 0,0001%, por ejemplo el yodo (I), el magnesio (Mg) o el cobalto (Co).
Los elementos traza y ultrataza pueden ser denominados en su conjunto, oligoelementos. Se han aislado 60 oligoelementos, pero de ellos solo 14 se consideran comunes en casi todos los seres vivos.
Proporción de los bioelementos
La proporción de los diversos bioelementos es muy diferente a la que hallamos en la atmósfera, la hidrosfera o la corteza terrestre; ellos indica que la vida
ha seleccionado aquellos elementos que le son más adecuados para formar
sus estructuras y realizar sus funciones. Por ejemplo, el carbono representa aproximadamente un 20% del peso de los organismos, pero su concentración en la atmósfera, en forma de dióxido de carbono es muy baja, de manera que los seres vivos extraen y concentran este elemento en sus tejidos.
La siguiente tabla muestra la proporción de algunos bioelementos en
el cuerpo humano comparada con la que tienen en el resto de la Tierra:3
| Elemento | Litosfera- atmósfera- hidrosfera (%) | Cuerpo humano (%) |
| Oxígeno (O) | 50,02 | 62,81 |
| Carbono (C) | 0,18 | 19,37 |
| Hidrógeno (H) | 0,95 | 9,31 |
| Nitrógeno (N) | 0,03 | 5,14 |
| Calcio (Ca) | 3,22 | 1,38 |
| Fósforo (P) | 0,11 | 0,64 |
| Azufre (S) | 0,11 | 0,63 |
| Sodio (Na) | 2,36 | 0,26 |
| Potasio (K) | 2,28 | 0,22 |
| Cloro (Cl) | 0,20 | 0,18 |
| Magnesio (Mg) | 2,08 | 0,04 |
| Flúor (F) | 0,10 | 0,009 |
| Hierro (Fe) | 4,18 | 0,005 |
| Aluminio (Al) | 7,30 | 0,001 |
| Manganeso (Mn) | 0,08 | 0,0001
|
| Silicio (Si) | 25,80 | — |
Tabla periódica y bioelementos
|
H |
He |
||||||||||||||||
|
Li |
Be |
B |
C |
N |
O |
F |
Ne |
||||||||||
|
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
||||||||||
|
K |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
|
Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
Xe |
|
Cs |
Ba |
La |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Hg |
Tl |
Pb |
Bi |
Po |
At Rn |
|
|
Fr |
Ra |
Ac |
|||||||||||||||
Biomolécula
Las biomoléculas son las moléculas constituyentes de los seres vivos. Los seis elementos químicos o bioelementos más abundantes en los seres vivos son el carbono, hidrógeno, oxígeno, nitrógeno, fósforo y azufre (C,H,O,N,P,S) representando alrededor del 99% de la masa de la mayoría de las células, con ellos se crean todo tipos de sustancias o biomoléculas (proteínas, aminoácidos, neurotransmisores).1 Estos seis elementos son los principales componentes de las biomoléculas debido a que:2
Las biomoléculas orgánicas pueden agruparse en cinco grandes tipos:
Algunas, como ciertos metabolitos (ácido pirúvico, ácido láctico, ácido cítrico, etcétera.) no encajan en ninguna de las anteriores categorías citadas.
Los requisitos mínimos diarios de las vitaminas no son muy altos, se necesitan tan solo dosis de miligramos o microgramos contenidas en grandes cantidades (proporcionalmente hablando) de alimentos naturales. Tanto la deficiencia como el exceso de los niveles vitamínicos corporales pueden producir enfermedades que van desde leves a graves e incluso muy graves como la pelagra o la demencia entre otras, e incluso la muerte. Algunas pueden servir como ayuda a las enzimas que actúan como cofactor, como es el caso de las vitaminas hidrosolubles
Existen compuestos orgánicos provenientes de los metabolitos primarios, que cumplen funciones complementarias a las vitales, tales como comunicación intra e interespecífica, defensa contra radiación, congelación, ataque de patógenos o parásitos. A estos compuestos se les denomina metabolitos secundarios.3
Los principales metabolitos secundarios comprenden:
- Permiten la formación de enlaces covalentes entre ellos, compartiendo electrones, debido a su pequeña diferencia de electronegatividad. Estos enlaces son muy estables, la fuerza de enlace es directamente proporcional a las masas de los átomos unidos.
- Permiten a los átomos de carbono la posibilidad de formar esqueletos tridimensionales –C-C-C- para formar compuestos con número variable de carbonos.
- Permiten la formación de enlaces múltiples (dobles y triples) entre C y C; C y O; C y N. Así como estructuras lineales, ramificadas, cíclicas, heterocíclicas, etc.
- Permiten la posibilidad de que con pocos elementos se den una enorme variedad de grupos funcionales (alcoholes, aldehídos, cetonas, ácidos, aminas, etc.) con propiedades químicas y físicas diferentes.
Clasificación de los biocompuestos
Según la naturaleza química, las biomoléculas son:Biocompuestos inorgánicos
Son moléculas que poseen tanto los seres vivos como los cuerpos inertes, aunque son imprescindibles para la vida, como el agua, la biomolécula más abundante, los gases (oxígeno, etc.) y las sales inorgánicas: aniones como fosfato (HPO4−), bicarbonato (HCO3−) y cationes como el amonio (NH4+).Biocompuestos orgánicos o principios inmediatos
Son sintetizadas principalmente por los seres vivos y tienen una estructura con base en carbono. Están constituidas, principalmente, por los elementos quimicos carbono, hidrógeno y oxígeno, y con frecuencia también están presentes nitrógeno, fósforo y azufre; a veces se incorporan otros elementos pero en mucha menor proporción.Las biomoléculas orgánicas pueden agruparse en cinco grandes tipos:
Glúcidos
Los glúcidos (impropiamente llamados hidratos de carbono o carbohidratos) son la fuente de energía primaria que utilizan los seres vivos para realizar sus funciones vitales; la glucosa está al principio de una de las rutas metabólicas productoras de energía más antigua, la glucólisis, usada en todos los niveles evolutivos, desde las bacterias a los vertebrados. Muchos organismos, especialmente los vegetales (algas, plantas) almacenan sus reservas en forma de almidón, en cambio los animales forman el glucógeno, entre ellos se diferencia por la cantidad y el número de ramificaciones de la glucosa. Algunos glúcidos forman importantes estructuras esqueléticas, como la celulosa, constituyente de la pared celular vegetal, o la quitina, que forma la cutícula de los artrópodos.Lípidos
Los lípidos saponificables cumplen dos funciones primordiales para las células; por una parte, los fosfolípidos forman el esqueleto de las membranas celulares (bicapa lipídica); por otra, los triglicéridos son el principal almacén de energía de los animales. Los lípidos insaponificables, como los isoprenoides y los esteroides, desempeñan funciones reguladoras (colesterol, hormonas sexuales, prostaglandinas).Proteínas
Las proteínas son las biomoléculas que más diversidad de funciones realizan en los seres vivos; prácticamente todos los procesos biológicos dependen de su presencia y/o actividad. Son proteínas casi todas las enzimas, catalizadores de reacciones metabólicas de las células; muchas hormonas, reguladores de actividades celulares; la hemoglobina y otras moléculas con funciones de transporte en la sangre; anticuerpos, encargados de acciones de defensa natural contra infecciones o agentes extraños; los receptores de las células, a los cuales se fijan moléculas capaces de desencadenar una respuesta determinada; la actina y la miosina, responsables finales del acortamiento del músculo durante el estado de la contracción; el colágeno, integrante de fibras altamente resistentes en tejidos de sostén de la planta y el talloÁcidos nucleicos
Los ácidos nucleicos, ADN y ARN, desempeñan, tal vez, la función más importante para la vida: contener, de manera codificada, las instrucciones necesarias para el desarrollo y funcionamiento de la célula. El ADN tiene la capacidad de replicarse, transmitiendo así dichas instrucciones a las células hijas que heredarán la información.Algunas, como ciertos metabolitos (ácido pirúvico, ácido láctico, ácido cítrico, etcétera.) no encajan en ninguna de las anteriores categorías citadas.
Vitaminas
Las vitaminas son precursoras de coenzimas, (aunque no son propiamente enzimas) grupos prostéticos de las enzimas. Esto significa, que la molécula de la vitamina, con un pequeño cambio en su estructura, pasa a ser la molécula activa, sea ésta coenzima o no.Los requisitos mínimos diarios de las vitaminas no son muy altos, se necesitan tan solo dosis de miligramos o microgramos contenidas en grandes cantidades (proporcionalmente hablando) de alimentos naturales. Tanto la deficiencia como el exceso de los niveles vitamínicos corporales pueden producir enfermedades que van desde leves a graves e incluso muy graves como la pelagra o la demencia entre otras, e incluso la muerte. Algunas pueden servir como ayuda a las enzimas que actúan como cofactor, como es el caso de las vitaminas hidrosolubles
Metabolitos secundarios
Las biomoléculas que son constituyentes fundamentales en procesos vitales de los seres vivos (mencionados anteriormente) son denominados metabolitos primarios. Estos metabolitos tienen distribución taxonómica amplia. Se puede considerar que los metabolitos primarios por excelencia son la glucosa, la ribosa, la fructosa, el ácido pirúvico, el gliceraldehído, el ácido acético (Esterificado como acetil coenzima A), el ácido oxaloacético, el ácido málico, el ácido 2-oxoglutárico, el ácido palmítico, el ácido esteárico, el ácido oleico, el porfibilinógeno, el pirofosfato de isopentenilo, los 20 aminoácidos proteínicos, las bases púricas, las bases pirimidínicas y las Vitaminas del grupo B.Existen compuestos orgánicos provenientes de los metabolitos primarios, que cumplen funciones complementarias a las vitales, tales como comunicación intra e interespecífica, defensa contra radiación, congelación, ataque de patógenos o parásitos. A estos compuestos se les denomina metabolitos secundarios.3
Los principales metabolitos secundarios comprenden:
-
- Policétidos y metabolitos secundarios de ácidos grasos
- Terpenos
- Metabolitos secundarios del ácido shikímico
- Aminoácidos no proteínicos
- Antibióticos peptídicos
- Glucósidos cianogénicos y glucosinolatos
- Metabolitos secundarios de la ruta del ácido cítrico
- Ciclitoles
- Alcaloides
BIOMOLECULAS ORGÁNICAS E INORGANICAS
La importancia de las biomoléculas:
Los ácidos
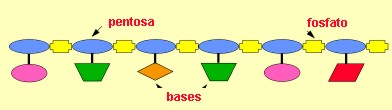
nucléicos son biomoléculas orgánicas conocidas como polirribonucleótidos o
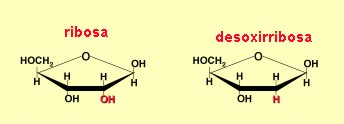
polidesoxirribonucleóticos, pues están formados por la repetición de unidades
moleculares llamadas nucleótidos. Hay dos tipos de ácidos nucléicos: el ácido
ribonucleico (ARN) y el ácido desoxirribonucleico (ADN).
Biomoléculas en los alimentos:
Carbohidratos
o glúcidos:
Los
carbohidratos o glúcidos son biomoléculas orgánicas compuestas por carbono,
hidrógeno y oxígeno. Son solubles en agua y se clasifican de acuerdo a la
cantidad de carbonos.
Lípidos:
Los lípidos
son un conjunto de biomoléculas orgánicas, compuestas principalmente por
carbono, hidrógeno y oxígeno, aunque también pueden contener fósforo, azufre y
nitrógeno, que tienen como característica principal el ser hidrofóbicas o
insolubles en agua. En el uso coloquial, a los lípidos se les llama
incorrectamente grasas, ya que las grasas son sólo un tipo de lípidos
procedentes de animales. Los lípidos cumplen funciones diversas en los
organismos vivientes, entre ellas la de reserva energética (triglicéridos), la
estructural (fosfolípidos) y la reguladora (esteroides).
Proteínas:
Las proteínas
son biomoléculas formadas por cadenas lineales de aminoácidos. Las proteínas
desempeñan un papel fundamental para la vida y son las biomoléculas más
versátiles y más diversas. Son imprescindibles para el crecimiento del
organismo y realizan una enorme cantidad de funciones diferentes.
Biomoléculas orgánicas e inorgánicas
¿Cómo se forman?
Todos los seres vivos presentamos
caracteristicas distintas a las de la materia inerte. Estas propiedades tienen
su origen en parte, en los atomos que conforman la materia viva, llamados
bioelementos.
En general,
los bioelementos más importantes para la vida se encuentran representados por
el carbono (C), el hidrogeno (H), el oxigeno (O) y el nitrogeno (N), los que
juntos pueden llegar a constituir el 99% de la masa de la celula.
Todos estos
elementos poseen caracteristicas especiales que explicarian el porque forman
parte fundamental de los seres vivos. Por ejemplo, tienen una masa atomica
reducida, y cuando se unen quimicamente, forman compuestos muy estables.
Otros
elementos importantes para los seres vivos son el sodio (Na), el potasio (K),
el cloro (Cl), el hierro (Fe) y el magnesio (Mg), por nombrar solo a algunos,
los que participan en funciones tan importantes como la conduccion nerviosa, el
moviemiento voluntario de los musculos, el transporte de oxigeno e incluso la
fotosintesis. Los bioelementos se combinan y dan origen a las biomoleculas,
mediante enlaces quimicos para formar distintos compuestos.
Biomoleculas
inorganicas:
Sales
minerales
GasesLípido
Los lípidos son un conjunto de moléculas orgánicas (la mayoría biomoléculas) compuestas principalmente por carbono e hidrógeno y en menor medida oxígeno, aunque también pueden contener fósforo, azufre y nitrógeno. Tienen como característica principal el ser hidrófobas (insolubles en agua) y solubles en disolventes orgánicos como la bencina, el benceno y el cloroformo. En el uso coloquial, a los lípidos se les llama incorrectamente grasas, ya que las grasas son sólo un tipo de lípidos procedentes de animales.Los lípidos cumplen funciones diversas en los organismos vivientes, entre ellas la de reserva energética (como los triglicéridos), la estructural (como los fosfolípidos de las bicapas) y la reguladora (como las hormonas esteroides).
Vitaminas
Las vitaminas son sustancias que el cuerpo
necesita para crecer y desarrollarse normalmente. Su cuerpo necesita 13
vitaminas. Son las vitaminas A, C, D, E, K y las vitaminas B (tiamina, riboflavina, niacina, ácido pantoténico, biotina, vitamina B-6, vitamina B-12 y folato o ácido fólico).
Por lo general, las vitaminas provienen de los alimentos que consume.
El cuerpo también puede producir vitaminas D y K. Las personas que
llevan una dieta vegetariana pueden necesitar un suplemento de vitamina B12.
Las vitaminas son substancias químicas no sintetizables por el organismo, presentes en pequeñas cantidades en los alimentos y
son indispensables para la vida, la salud, la actividad física y cotidiana.
Las vitaminas no producen energía y por tanto no implican calorías. Intervienen como catalizador en las reacciones bioquímicas provocando la liberación de energía. En otras palabras, la función de las vitaminas es la de facilitar la transformación que siguen los sustratos a través de las vías metabólicas.
Identificar las vitaminas ha llevado a que hoy se reconozca, por ejemplo, que en el caso de los deportistas haya una mayor demanda vitamínica por el incremento en el esfuerzo físico, probándose también que su exceso puede influir negativamente en el rendimiento.
Conociendo la relación entre el aporte de nutrientes y el aporte energético, para asegurar el estado vitamínico correcto, es siempre más seguro privilegiar los alimentos de fuerte densidad nutricional (legumbres, cereales y frutas) por sobre los alimentos meramente calóricos.
Las vitaminas se dividen en dos grandes grupos:
Vitaminas Liposolubles: Aquellas solubles en cuerpos lípidos.
Vitaminas Hidrosolubles: Aquellas solubles en líquidos.
Descubriendo las vitaminas
Entre los años 1906 y 1912 el gran bioquímico inglés Sir Frederick Hopkins, fue quien propuso para esas sustancias desconocidas que hoy llamamos vitaminas el nombre de "factores accesorios de la alimentación".
Todo se inicio cuando comenzaron a estudiar el porque se producían ciertas enfermedades y se llego a la conclusión de que las diferentes dolencias se generaban por la falta de algunas sustancias: carencias.
En aquellos años no se conocía la estructura química de las vitaminas, pero si se sabia que algunas aparecían asociadas a los componentes grasos de los alimentos (vitaminas liposolubles), y otras a la parte acuosa (vitaminas hidrosolubles).
El descubrimiento de las vitaminas ha escrito una de las páginas más brillantes de la ciencia moderna y ha sido el resultado de la estrecha colaboración entre las distintas disciplinas científicas.
Las vitaminas son fundamentales para las diferentes especies, puesto que no pueden sintetizarse en el organismo y eso es justamente lo que la define como tal: la necesidad de su presencia en la dieta.
Las cantidades necesarias son diferentes según sea el sexo y la edad de la persona; y en el caso de las mujeres también cambia durante el embarazo y la lactancia. Sus valores se expresan en diferentes unidades, generalmente microgramos (µg) o miligramos (mg.) según sea la vitamina de la que se habla, pero también se puede encontrar indicada en unidades internacionales (UI).
Existe un número de actividades cotidianas que interfieren al buen estado nutricional y vitamínico, a los cuales se los debe considerar como contrarios a las vitaminas, y están comprendidas principalmente por el consumo de tabaco, alcohol, café y te en exceso, ciertos medicamentos y los métodos de cocción de los alimentos que afectan a su conservación. Algunas personas cuentan con carencias vitamínicas sistemáticas, y son candidatos a predisponerse a problemas por carencia de atención a falencias alimenticias. A este grupo de riesgo puede considerárselo frecuentemente como víctimas de este tipo de problemas.
La prescripción dietética médica apuntará a favorecer el enriquecimiento de la alimentación, según las necesidades individuales y sin favorecer calorías o desequilibrios en forma inapropiada.
Exceso de vitaminas o hipervitaminosis
Así como son indispensables para el organismo, el exceso de vitaminas puede tener efectos graves sobre la salud. A esto se llama hipervitaminosis. En muchos casos el exceso puede ser tóxico para el organismo, por tanto se debe tener cuidado especialmente cuando se suplementa a una persona con vitaminas.
Por lo general, una persona que lleva una alimentación normal o completa, nunca presenta carencia o exceso de vitaminas.
Los casos particulares al exceso de cada vitamina, a como el organismo los demuestra y a sus posibles consecuencias, vea la página de cada vitamina y consulte además a su médico.
Compuestos considerados 'cuasi-vitaminas'
Existen otros componentes, especificamente ácidos considerados vitaminas que se consideraban pertenecientes al grupo B de vitaminas hidrosolubles, que aportan importantes nutrientes al organismo. Si bien se demostró que estos no son vitaminas, si se ha establecido que son muy útiles al organismo y metabolismo.
Cada vitamina tiene funciones específicas. Si tiene bajos niveles de
determinadas vitaminas, puede desarrollar una enfermedad por
deficiencia. Por ejemplo, si no recibe suficiente vitamina D, podría
desarrollar raquitismo. Algunas vitaminas pueden ayudar a prevenir los
problemas médicos. La vitamina A previene la ceguera nocturna.
La mejor manera de obtener suficientes vitaminas es mantener una dieta balanceada con alimentos variados. En algunos casos, es posible que se necesite un multivitamínico diario para una salud óptima. Sin embargo, las altas dosis de algunas vitaminas pueden enfermarlo.
La mejor manera de obtener suficientes vitaminas es mantener una dieta balanceada con alimentos variados. En algunos casos, es posible que se necesite un multivitamínico diario para una salud óptima. Sin embargo, las altas dosis de algunas vitaminas pueden enfermarlo.
Las vitaminas no producen energía y por tanto no implican calorías. Intervienen como catalizador en las reacciones bioquímicas provocando la liberación de energía. En otras palabras, la función de las vitaminas es la de facilitar la transformación que siguen los sustratos a través de las vías metabólicas.
Identificar las vitaminas ha llevado a que hoy se reconozca, por ejemplo, que en el caso de los deportistas haya una mayor demanda vitamínica por el incremento en el esfuerzo físico, probándose también que su exceso puede influir negativamente en el rendimiento.
Conociendo la relación entre el aporte de nutrientes y el aporte energético, para asegurar el estado vitamínico correcto, es siempre más seguro privilegiar los alimentos de fuerte densidad nutricional (legumbres, cereales y frutas) por sobre los alimentos meramente calóricos.
Las vitaminas se dividen en dos grandes grupos:
Vitaminas Liposolubles: Aquellas solubles en cuerpos lípidos.
 |
 |
 |
 |
| Vitamina A | Vitamina D | Vitamina E | Vitamina K |
 |
 |
 |
 |
 |
 |
| Vitamina B1 | Vitamina B2 | Vitamina B3 | Vitamina B6 | Vitamina B12 | Vitamina C |
Descubriendo las vitaminas
Entre los años 1906 y 1912 el gran bioquímico inglés Sir Frederick Hopkins, fue quien propuso para esas sustancias desconocidas que hoy llamamos vitaminas el nombre de "factores accesorios de la alimentación".
Todo se inicio cuando comenzaron a estudiar el porque se producían ciertas enfermedades y se llego a la conclusión de que las diferentes dolencias se generaban por la falta de algunas sustancias: carencias.
En aquellos años no se conocía la estructura química de las vitaminas, pero si se sabia que algunas aparecían asociadas a los componentes grasos de los alimentos (vitaminas liposolubles), y otras a la parte acuosa (vitaminas hidrosolubles).
El descubrimiento de las vitaminas ha escrito una de las páginas más brillantes de la ciencia moderna y ha sido el resultado de la estrecha colaboración entre las distintas disciplinas científicas.
Principales funciones de las vitaminas
| Vitamina A |
Es necesaria para el crecimiento y desarrollo de huesos.
Escencial para el desarrollo celular Ayuda al sistema inmune Es fundamental para la visión, el Retinol contribuye a mejorar la visión nocturna Antioxidante |
| Vitamina B1 |
En la transformación de los alimentos en energía
Absorción de glucosa por parte del sistema nervioso |
| Vitamina B2 |
Interviene en la transformación de los alimentos en energía
Ayuda a conservar una buena salud visual. Conserva el buen estado de las células del sistema nervioso. Interviene en la regeneración de los tejidos de nuestro organismo (piel, cabellos, uñas) Produce glóbulos rojos junto a otras vitaminas del complejo B, y en conjunto con la niacina y piridoxina mantiene al sistema inmune en perfecto estado. Complementa la actividad antioxidante de la vitamina E. |
| Vitamina B3 |
Obtención de energía a partir de los glúcidos o hidratos de carbono.
Mantiene el buen estado del sistema nervioso junto a la piridoxina (vitamina B6) y la riboflavina (vitamina B2). Mejora el sistema circulatorio Mantiene la piel sana mantiene sanas las mucosas digestivas. Estabiliza la glucosa en sangre. |
| Vitamina B6 |
Interviene en la transformación de hidratos de carbono y grasas en energía
Interviene en el proceso metabólico de las proteínas Mejora la circulación general Ayuda en el proceso de producción de ácido clorhídrico en el estómago Mantiene el sistema nervioso en buen estado Mantiene el sistema inmune Interviene en la formación de hemoglobina en sangre Es fundamental su presencia para la formación de Niacina o vitamina B3 Ayuda a absorber la vitamina B12 o cobalamina. |
| Vitamina B12 |
Interviene en la síntesis de ADN, ARN y proteínas
Interviene en la formación de glóbulos rojos. Mantiene la vaina de mielina de las células nerviosas Participa en la síntesis de neurotransmisores Es necesaria en la transformación de los ácidos grasos en energía Ayuda a mantener la reserva energética de los músculos Interviene en el buen funcionamiento del sistema inmune Es necesaria para el metabolismo del ácido fólico. |
| Vitamina C |
Antioxidante
Mejora la visión Es antibacteriana, por lo que inhibe el crecimiento de ciertas bacterias dañinas para el organismo. Repara y mantiene cartílagos, huesos y dientes. Reduce las complicaciones derivadas de la diabetes tipo II Disminuye los niveles de tensión arterial y previene la aparición de enfermedades vasculares Tiene propiedades antihistamínicas Ayuda a prevenir o mejorar afecciones de la piel como eccemas o soriasis. Es imprescindible en la formación de colágeno. Aumenta la producción de estrógenos durante la menopausia Mejora el estreñimiento por sus propiedades laxantes. |
| Vitamina D |
El rol más importante de esta vitamina es mantener los niveles de calcio y fósforo normales.
Participa en el crecimiento y maduración celular. Fortalece al sistema inmune ayudando a prevenir infecciones. |
| Vitamina E |
Es un antioxidante natural
Cumple un rol importante en cuanto al mantenimiento del sistema inmune saludable Protege al organismo contra los efectos del envejecimiento. Es esencial en el mantenimiento de la integridad y estabilidad de la membrana axonal (membrana de las neuronas). Previene la trombosis. Es importante en la formación de fibras elásticas y colágenas del tejido conjuntivo. Promueve la cicatrización de quemaduras. Protección contra la destrucción de la vitamina A, selenio, ácidos grasos y vitamina C. Protección contra la anemia. |
| Vitamina K |
Coagulación sanguínea
Participa en el metabolismo oseo ya que una proteína ósea llamada osteocalcina requiere de la vitamina K para su maduración. |
| Acidos previamente considerados vitaminas | |
| Acido Fólico (Vitamina B9) |
Participa en el metabolismo del ADN, ARN y proteínas,
Necesario para la formación de glóbulos rojos, Reduce el riesgo de aparición de defectos del tubo neural del futuro bebé como lo son la espina bífida y la anencefalia, Disminuye la ocurrencia de enfermedades cardiovasculares, Previene algunos tipos de cáncer, Estimula la formación de ácidos digestivos. |
| Acido Pantotenico (Vitamina B5) |
Forma parte de la Coenzima A.
Interviene en la síntesis de hormonas antiestrés (adrenalina) en las glándulas suprarrenales, a partir del colesterol. Interviene en el metabolismo de proteínas, hidratos de carbono y grasas. Es necesaria para la formación de anticuerpos Interviene en la síntesis de hierro. Interviene en la formación de insulina. Ayuda a aliviar los síntomas de la artritis. Reduce la acidez estomacal junto a la biotina y la tiamina. Ayuda a disminuir los niveles de colesterol en sangre. Mejorar y aliviar trastornos ocasionados por el estrés. Mejora algunas afecciones de la piel. |
| Biotina (Vitamina B8) |
Interviene en la formación de hemoglobina.
Interviene en procesos celulares a nivel genético. Interviene en el proceso de obtención de energía a partir de la glucosa. Es necesaria su presencia para la correcta metabolizacion de hidratos de carbono, proteínas y lípidos. Funciona en conjunto con el ácido fólico y el ácido pantoténico. Mantiene las uñas, piel y cabellos sanos. Ayuda a prevenir la neuropatía diabética y estabiliza los niveles de azúcar en sangre (glucemia). |
| Carnitina (Vitamina B11) |
Participa en la metabolización de grasas para producir energía.
Mejora la circulación sanguínea. Desintoxica a nuestro organismo del amoníaco, sustancia que deriva de la descomposición de las proteínas. Falicita la oxidación de la glucosa. Disminuye el riesgo de depósitos grasos en el hígado. |
Los requerimientos diarios y el estado nutricional
Las vitaminas son fundamentales para las diferentes especies, puesto que no pueden sintetizarse en el organismo y eso es justamente lo que la define como tal: la necesidad de su presencia en la dieta.
Una persona que lleva una alimentación normal o completa, nunca presenta carencia o exceso de vitaminas.
El requerimiento diario de vitaminas que el organismo necesita ha sido establecido cientificamente tras años de investigación.
Las cantidades necesarias son diferentes según sea el sexo y la edad de la persona; y en el caso de las mujeres también cambia durante el embarazo y la lactancia. Sus valores se expresan en diferentes unidades, generalmente microgramos (µg) o miligramos (mg.) según sea la vitamina de la que se habla, pero también se puede encontrar indicada en unidades internacionales (UI).
| Requerimiento diario de: | Hombres | Mujeres |
| Vitamina A | 900 µg | 700 µg |
| Vitamina D | 5 µg | |
| Vitamina E | 15 mg | |
| Vitamina K | 120 mg | 90 mg |
| Vitamina B1 | 1.2 mg | 1.1 mg |
| Vitamina B2 | 1.3 mg | 1.1 mg |
| Vitamina B3 | 16 mg | 14 mg |
| Vitamina B6 | 1.3 mg | |
| Vitamina B12 | 2.4 µg | 2.4 µg |
| Vitamina C | 90 mg | 75 mg |
| La tabla muestra los requerimientos diarios de vitaminas para una persona promedio con edad entre 19 y 50 años segun el departamento de nutrición del IOM (Institute of Medicine - Instituto de Medicina) y la USDA (United States Department of Agriculture). | ||
| Para ver en detalle los requerimientos diarios que corresponden a cada vitamina clickee sobre la vitamina correspondiente en la
columna izquierda de la tabla.
µg son microgramos. mg son miligramos. | ||
Existe un número de actividades cotidianas que interfieren al buen estado nutricional y vitamínico, a los cuales se los debe considerar como contrarios a las vitaminas, y están comprendidas principalmente por el consumo de tabaco, alcohol, café y te en exceso, ciertos medicamentos y los métodos de cocción de los alimentos que afectan a su conservación. Algunas personas cuentan con carencias vitamínicas sistemáticas, y son candidatos a predisponerse a problemas por carencia de atención a falencias alimenticias. A este grupo de riesgo puede considerárselo frecuentemente como víctimas de este tipo de problemas.
La prescripción dietética médica apuntará a favorecer el enriquecimiento de la alimentación, según las necesidades individuales y sin favorecer calorías o desequilibrios en forma inapropiada.
Exceso de vitaminas o hipervitaminosis
Así como son indispensables para el organismo, el exceso de vitaminas puede tener efectos graves sobre la salud. A esto se llama hipervitaminosis. En muchos casos el exceso puede ser tóxico para el organismo, por tanto se debe tener cuidado especialmente cuando se suplementa a una persona con vitaminas.
Por lo general, una persona que lleva una alimentación normal o completa, nunca presenta carencia o exceso de vitaminas.
Los casos particulares al exceso de cada vitamina, a como el organismo los demuestra y a sus posibles consecuencias, vea la página de cada vitamina y consulte además a su médico.
Compuestos considerados 'cuasi-vitaminas'
Existen otros componentes, especificamente ácidos considerados vitaminas que se consideraban pertenecientes al grupo B de vitaminas hidrosolubles, que aportan importantes nutrientes al organismo. Si bien se demostró que estos no son vitaminas, si se ha establecido que son muy útiles al organismo y metabolismo.
Enzima

Estructura de la triosafosfato isomerasa. Conformación en forma de diagrama de cintas rodeado por el modelo de relleno de espacio de la proteína. Esta proteína es una eficiente enzima involucrada en el proceso de transformación de azúcares en energía en las células.
Debido a que las enzimas son extremadamente selectivas con sus sustratos y su velocidad crece sólo con algunas reacciones, el conjunto (set) de enzimas sintetizadas en una célula determina el tipo de metabolismo que tendrá cada célula. A su vez, esta síntesis depende de la regulación de la expresión génica.
Como todos los catalizadores, las enzimas funcionan disminuyendo la energía de activación (ΔG‡) de una reacción, de forma que se acelera sustancialmente la tasa de reacción. Las enzimas no alteran el balance energético de las reacciones en que intervienen, ni modifican, por lo tanto, el equilibrio de la reacción, pero consiguen acelerar el proceso incluso millones de veces. Una reacción que se produce bajo el control de una enzima, o de un catalizador en general, alcanza el equilibrio mucho más deprisa que la correspondiente reacción no catalizada.
Al igual que ocurre con otros catalizadores, las enzimas no son consumidas por las reacciones que catalizan, ni alteran su equilibrio químico. Sin embargo, las enzimas difieren de otros catalizadores por ser más específicas. Las enzimas catalizan alrededor de 4 000 reacciones bioquímicas distintas.4 No todos los catalizadores bioquímicos son proteínas, pues algunas moléculas de ARN son capaces de catalizar reacciones (como la subunidad 16S de los ribosomas en la que reside la actividad peptidil transferasa).5 6 También cabe nombrar unas moléculas sintéticas denominadas enzimas artificiales capaces de catalizar reacciones químicas como las enzimas clásicas.7
La actividad de las enzimas puede ser afectada por otras moléculas. Los inhibidores enzimáticos son moléculas que disminuyen o impiden la actividad de las enzimas, mientras que los activadores son moléculas que incrementan dicha actividad. Asimismo, gran cantidad de enzimas requieren de cofactores para su actividad. Muchas drogas o fármacos son moléculas inhibidoras. Igualmente, la actividad es afectada por la temperatura, el pH, la concentración de la propia enzima y del sustrato, y otros factores físico-químicos.
Algunas enzimas son usadas comercialmente, por ejemplo, en la síntesis de antibióticos y productos domésticos de limpieza. Además, son ampliamente utilizadas en diversos procesos industriales, como son la fabricación de alimentos, destinción de vaqueros o producción de biocombustibles.
Las enzimas
La Enzima Como Unidad Fundamental De VidaCada célula y cada tejido tienen su actividad propia, lo que comporta continuos cambios en su estado bioquímico, en la base de la cual están las enzimas, que tienen el poder de catalizar, facilitar, y agilizar determinados procesos sintéticos y analíticos. Los propios genes son reguladores de la producción de las enzimas; por tanto, genes y enzimas pueden considerados como las unidades fundamentales de la vida.
Este concepto poco difundido casi hasta el siglo XX, se ha desarrollado y concretado cada vez mas, y constituye un componente esencial de diversas disciplinas: la microbiología, la fisiología, la bioquímica, la inmunología y la taxonomía, formando además parte del campo aplicado, en gran variedad de industrias. El rasgo particular de las enzimas es que pueden catalizar procesos químicos a baja temperatura, compatible con la propia vida, sin el empleo de sustancias lesivas para los tejidos. La vida es, en síntesis, una cadena de procesos enzimáticos, desde aquellos que tienen por sustratos los materiales mas simples, como el agua (H2O) y el anhídrido carbónico (CO2), presentes en los vegetales para la formación de hidratos de carbono, hasta los mas complicados que utilizan sustratos muy complejos.
La formación de los prótidos, los glúcidos y los lípidos es un ejemplo típico: Son a la vez degradados y reconstruidos por otras reacciones enzimáticas, produciendo energía a una velocidad adecuada para el organismo, sin el gasto energético que exigen los métodos químicos de laboratorio.
4. Importancia biomedica de las enzimas
Sin enzimas, no sería posible la vida que conocemos. Igual que la biocatálisis que regula la velocidad a la cual tienen lugar los procesos fisiológicos, las enzimas llevan a cabo funciones definitivos relacionadas con salud y la enfermedad. En tanto que, en la salud todos los procesos fisiológicos ocurren de una manera ordenada y se conserva la homeostasis, durante los estados patológicos, esta última puede ser perturbada de manera profunda. Por ejemplo, el daño tisular grave que caracteriza a la cirrosis hepática pueden deteriorar de manera notable la propiedad de las células para producir enzimas que catalizan procesos metabólicos claves como la síntesis de urea. La incapacidad celular para convertir el amoniaco tóxico a urea no tóxica es seguida por intoxicación con amoniaco y por ultimo coma hepático. Un conjunto de enfermedades genéticas raras, pero con frecuencia debilitantes y a menudo mortales, proporciona otros ejemplos dramáticos de las drásticas consecuencias fisiológicas que pueden seguir al deterioro de la actividad enzimática, inclusive de una sola enzima.
Después del daño tisular grave (por ejemplo, infarto del miocardio o pulmonar, trituración de un miembro) o siguiendo a multiplicación celular descontrolada (por ejemplo, carcionoma prostatico), las enzimas propias de tejidos específicos pasan a la sangre. Por lo tanto, la determinacion de estas enzimas intracelulares en el suero sanguineo proporciona a los medicos informacion valiosa para el diagnostico y el pronostico.
5. Caracteristicas de las enzimas
Desde el punto de vista químico, las enzimas están formadas de carbono (C), Hidrógeno (H), oxigeno (O), Nitrógeno (Ni), y Azufre (S) combinados, pero siempre con peso molecular bastante elevado y común propiedades catálicas especificas. Su importancia es tal que puede considerarse la vida como un "orden sistemático de enzimas funcionales". Cuando este orden y su sistema funcional son alterados de algún modo, cada organismo sufre mas o menos gravemente y el trastorno puede ser motivado tanto por la falta de acción como por un exceso de actividad de enzima.
Las enzimas son catalizadores de naturaleza proteínica que regulan la velocidad a la cual se realizan los procesos fisiologicos, producidos por los organismos vivos. En consecuencia, las deficiencias en la funcion enzimatica causan patologias.
Las enzimas, en los sistemas biológicos constituyen las bases de las complejas y variadas reacciones que caracterizan los fenómenos vitales. La fijación de la energía solar y la síntesis de sustancias alimenticias llevadas a cabo por los vegetales dependen de las enzimas presentes en las plantas. Los animales, a su vez, están dotados de las enzimas que les permiten aprovechar los alimentos con fines energéticos o estructurales; las funciones del metabolismo interno y de la vida de relación, como la locomoción, la excitabilidad, la irritabilidad, la división celular, la reproducción, etc. Están regidas por la actividad de innumerables enzimas responsables de que las reacciones se lleven a cabo en condiciones favorables para el individuo, sin liberaciones bruscas de energía a temperaturas fijas en un medio de pH, concentración salina, etc.; prácticamente constante.
A diferencia de un catalizador inorgánico que interviene en numerosas reacciones las enzimas producidas por los organismos vivos habitualmente solo catalizan un tipo de reacción o solo una reacción determinada; la especificidad de las enzimas es tan marcadas que en general actúan exclusivamente sobre sustancias que tienen una configuración precisa; por ejemplo, si solo atacan a los aminoácidos que tienen su carbono a , asimétrico, con estructura L-, no muestran la menor actividad sobre formas idénticas de dichos aminoácidos, pero que sean del tipo D-.
En los sistemas biológicos se llevan a cabo diversas reacciones a partir de la misma sustancia; por ejemplo algunos microorganismos convierten la glucosa en alcohol y bióxido de carbono, al paso que otros gérmenes la convierten en ácido láctico o ácido pirúvico o acetaldehido. Esto quiere decir que la glucosa puede descomponerse en distintos productos y aunque todas las posibilidades son teóricas y prácticamente posibles la presencia de ciertas enzimas favorece uno de los caminos que llevan a la acumulación de determinados compuestos.
Las enzimas, por lo tanto, se consideran como catalizadores altamente específicos que:
- Modifican la velocidad de los cambios promovidos por ellas.
- Determinan que sustancias particulares, de preferencia a otras distintas son las que van a sufrir los cambios.
- Impulsan dentro de los distintos cambios posibles que pueda seguir una sustancia, cual de ellos en especial, será el utilizado.
6. La estructura enzimática
Por su estructura y composición química puede afirmarse que el origen de las enzimas esta vinculando al origen de las sustancias proteicas. Al hablar del origen de la vida se ha citado el éxito de los experimentos realizados en el laboratorio para la producción de aminoácidos; estos aminoácidos son los que precisamente constituyen la base del edificio proteico. También en el laboratorio se ha intentado la síntesis de proteínas a partir de aminoácidos.
La sede de las enzimas es el citoplasma. Los cloroplastos vegetales contienen una amplia gama enzimas encargadas de la función clorofílica, proceso que a través de reacciones químicas complejas y encadenadas transforman compuestos inorgánicos, como el agua, y el anhídrido carbónico, en sustancias complejas adecuadas para ser entre otras cosas el alimento fundamental de los animales.
En las mitocondrias existe un sistema de transporte de electrones que determinan importantes fenómenos de oxidorreducción, durante los cuales se forman notables cantidades de ATP, que es un compuesto altamente energético del que depende la mayor parte de metabolismo, y coma, por tanto el trabajo de las células; en las mitocondrias se produce el metabolismo enzimático de los ácidos grasos, los cuales son en parte elaborados también en el citoplasma.
En los ribosomas tiene lugar concretamente todas la s síntesis de las sustancias proteicas, mientras que en los lisosomas se producen enzimas hidrolíticos cuya misión escindir, con la intervención del agua, moléculas grandes en otras menores, que pueden a su vez ser utilizadas por las células; en cambio, las enzimas glucolíticos están difundidos en el citoplasma.
La localización de las sedes de las distintas operaciones enzimáticas antes mencionadas ha sido posible a través del sistema de ruptura de las células y de la separación de los distintos componentes mediante centrifugación diferencial del homogeneizado de estas la ruptura celular y la subdivisión de los componentes subcelulares se realizan actualmente utilizando los tejidos, por ejemplo con saltos bruscos desde temperaturas inferiores a 0° C hasta temperaturas mas elevadas con cambios de presión osmótica o mediante ultrasonidos.
7. Naturaleza química de las enzimas
Existen numerosas razones para afirmar que las enzimas son proteinas. La
más importantes son las siguientes:
- El análisis de las enzimas obtenidas en forma más pura, criatalizada, demuestra que son proteínas.
- Las enzimas son inactivadas a altas temperaturas y, en geeral, la cinética de la desnaturalización térmica de las enzimas da resultados muy parecidos a los de la desnaturalización térmica de las proteínas; por ejemplo el Q10 de la mayoría de las reacciones químicas es de 2 a 3, y, en el casod e las enzimas, a temperaturas elevadas, alrededor de 60 a 70 ° C, la actividad neta aumeta varios cientos, como sucede con la velocidad de la desnaturalización térmica de las proteínas.
- Las enzimas son activadas en unas zona muy restringida de pH, y presenta un punto óptimo de ph donde su actividad es mayor. Las proteínas en su punto isoeléctrico, muestran propiedades parecidas desde el punto de vista de viscosidad, solubilidad, difución, etc., que resulta del todo similares a las propiedades de este tipo que muestran las enzimas.
- Todos los agentes que desnaturalizan a las proteínas también destruyen o inactivan a las enzimas, ya sea el calor, los ácidos fuertes, o los metales pesados que puedesn combinarse con ellas.
- Los problemas de solubilidad y de precipitación son comunes a las proteínas y las enzimas; en general, son solubles en agua o soluciones salinas, insolubles en alcohol, precipitan con determinadas concentraciones de sales neutras, etc.
Los conocimientos sobre la composición química de las enzimas constituyeron materia de numerosas controversias hasta 1926, cuando J.B Sumner (1887-1955) consiguió cristalizar la ureasa, enzima que transforma la urea en anhídrido carbonico y amoniaco, y demostrar que era una sustancia proteica.
A, partir de entonces fueron aisladas otras enzimas en forma pura, cristalina, y el análisis demostraba siempre la presencia de una proteina, simple o conjugada. Cuando los analisi químicos demuestran que la enzima es una proteína conjugada, pueden distinguirse en el dos partes bien diferenciadas:
- El grupo prosteico (Coenzima)
- La proteina (Apoenzima)
- Solo proteínas, que difieren entre si por la secuencia con que los aminoácidos están combinados, como la ureasa y las enzimas digestivas (la pepsina y la tripsina)
- Los conjugados, separados en dos entidades químicas bien definidas: la coenzima y la apoenzima.
9. Nomenclatura y clasificacion de las enzimas
Cien años atrás solo se conocian enzimas, muchas de estas, catalizaban la hidrólisis de enlaces covalentes. Algunas enzimas, de manera especial las que fueron descubiertas en un principio, recibieron nombres ligados mas bien a su sitio de procedencia anatómica que no siguen ninguna regla ni sistema; tal es el caso de la ptialina de la saliva, que ataca al almidón de la pepsina del estómago y de la tripsina del páncreas, que atacan proteínas; de la renina, que cuagula la leche; de la papaina, enzima proteolítica que se encuentra en la papaya y de las catepsinas, también proteasas, que se encuentran en las células. Las enzimas relacionadas con la cuagulación de la sangre, como son la trombina, la plasmina, el plasminógeno, etc. reciben también nombres sistematizados.
Al descrubir nuevas enzimas y proceder a su caracterización estricta se aplicaron reglas de nomenclatura basadas en el nombre del sustrato atacado, o en el tipo general de sustrato, o en la reacción catalizada y se ha añadido convencionalmente, la terminación -asa. Por ejemplo: las lipasas (hidrolizan lipidos o grasas), las amilasas (hidrolizan almidon), las proteasas (hidrolizan proteinas), las esterasas (basado en la unión general de tipo éster presentes en muchas sustancias), colesterol estrerasa (si la esterasa es específica de los esteres de colesterol) y acetilcolina esterasa (si la estersa de la acetilcolina). Otros ejemplos: Las fosfatasas son enzimas que atacan las uniones éster, pero en este caso, toman su nombre del grupo vecino a la unión que van a atacar, de manera que se denominan fosfatasas (cuando quitan una molécula de monofosfato), pirofosfatasas (cuando quitan el ácido fosfórico como esteres dobles (pirofosfatos), o triples, etc.) De la misma manera, las carbohidrasas se denominan así genericamente, pero pueden comprender enzimas con nombres proveniente del sustrato particular sobre el que actuan como la amilasa que ataca al almidón y la celulasa que actúa sobre la celulosa y, en otras ocaciones, se denominan de acuerdo con la unión atacada, como la b -glucosidasa que actúa sobre las uniones b -glucosídicas. Los ejemplos se pueden extender a todos los terrenos de la actividad enzimática, como en las enzimas proteolíticas, las fosforilasas, las nucleasas, etc.
Esta manera de llamarlas, se demostro que era inadecuada porque al descubrirse varias enzimas, notaron que varias enzimas catalizaban reacciones diferentes del mismo sustrato, por ejemplo, oxidacion o reduccion de la funcion alcohol de un azucar.
Aunque el sufijo –asa continua en uso; actualmente, al nombrar a las enzimas, se enfatiza el tipo de reaccion catalizada. Por ejemplo: las hidrogenasas catalizan la eliminacion de hidrogeno y las transferasas, reacciones de transferencia de grupo. Con el descubrimiento de mas y mas enzimas, surgieron ambiguedades y con frecuencia no estaba claro cual era la enzima que un investigador deseaba estudiar. Para remediar esta deficiencia, la Comisión para el estudio de las enzimas, que constituye con respecto a los sistemas anteriores un punto de vista más uniforme, preciso y descriptivo; esta formada por la Union Internacional de Bioquimica (IUB) adopto, en 1964, un sistema complejo pero inequivoco de la nomenglatura enzimatica basado en el mecanismo de reaccion.
El sistema se basa en la reacción química catalizada que es la propiedad específica que caracteriza a cada enzima las cuales se agrupan en clases, porque catalizan procesos semejantes, y en subclases que especifican con mayor exactitud la reacción particular considerada. En general, las enzimas reciben un nombre de acuerdo con el sustrato o los sustratos que participan en la reacción seguido por el tipo de reacción catalizada y, por fin, la terminación -asa. A menudo los nombres así obtenidos resultan largos y complejos, por lo que es muy dificil que en la práctica se pueda excluir el uso de los nombres triviales, consagrados por la costumbre. Sin embargo, con fines de sistematización, se reconoce la necesidad de aceptar el nuevo sistema.
Aunque su claridad y carencia de ambigüedad recomiendan al sistema de nomenglatura IUB para trabajos de investigacion, nombres mas ambiguos, pero basante mas cortos persisten en libros de texto y en el laboratorio clinico. Por esta razon, a continuacion solo se presenta principios generales del sistema IUB:
- Las reacciones y las enzimas que las catalizan se dividen en 6 clases principales, cada una con 4 a 13 subclases.
- El nombre de la enzima tiene 2 partes: la primera es el nombre del o los sustratos; la segunda, con terminacion –asa, indica el tipo de reaccion catalizada.
- Informacion adicional, si es necesario aclarar la reaccion, puede seguir el parentesis. Por ejemplo: la enzima que cataliza L-malato + NAD= = piruvato + CO2 NADH + H= , se denomina como 1.1.1.37 L-malato:NAD+ oxidorreductasa (descarboxilante).
- Cada enzima tiene un numero clave (E.C.) que caracteriza al tipo de reaccion según la clase (primer digito), subclase (segundo digito) y subclase (tercer digito). El cuarto digito es para la enzima especifica. Asi, E.C. 2.7.1.1 denota la clase 2 (una transferasa), subclase 7 (transferencia de fosfato), sub-clase 1 (una funcion alcohol como aceptor de fosfato). El ultimo digito denota a la enzima hexocinasa o ATP: D-hexosa-6-fosforotransferasa, enzima que cataliza la transferencia de fosfato desde el ATP al grupo hidroxilo de carbono 6 de la glucosa.
- Oxidoreductasas
- Transferasas
- Hidrolasas
- Isomerasa
- Liasas
En esta clase se encuentran las siguientes subclases principales: Deshidrogenasas y oxidasas. Son más de un centenar de enzimas en cuyos sistemas actúan como donadores, alcoholes, oxácidos aldehidos, cetonas, aminoácidos, DPNH2, TPNH2, y muchos otros compuestos y, como receptores, las propias coenzimas DPN y TPN, citocromos, O2, etc.
2.Las Transferasas: Estas enzimas catalizan la transferencia de una parte de la molécula (dadora) a otra (aceptora). Su clasificación se basa en la naturaleza química del sustrato atacado y en la del aceptor. También este grupo de enzimas actúan sobre los sustratos mas diversos, transfiriendo grupos metilo, aldehído, glucosilo, amina, sulfató, sulfúrico, etc.
3.Las Hidrolasas: Esta clase de enzimas actúan normalmente sobre las grandes moléculas del protoplasma, como son la de glicógeno, las grasas y las proteínas. La acción catalítica se expresa en la escisión de los enlaces entre átomos de carbono y nitrógeno (C-Ni) o carbono oxigeno (C-O); Simultáneamente se obtiene la hidrólisis (reacción de un compuesto con el agua)de una molécula de agua. El hidrógeno y el oxidrilo resultantes de la hidrólisis se unen respectivamente a las dos moléculas obtenidas por la ruptura de los mencionados enlaces. La clasificación de estas enzimas se realiza en función del tipo de enlace químico sobre el que actúan.
A este grupo pertenecen proteínas muy conocidas: la pepsina, presente en el jugo gástrico, y la tripsina y la quimiotripsina, segregada por el páncreas. Desempeñan un papel esencial en los procesos digestivos, puesto que hidrolizan enlaces pépticos, estéricos y glucosídicos.
4.Las isomerasas:Transforman ciertas sustancias en otras isómeras, es decir, de idéntica formula empírica pero con distinto desarrollo. Son las enzimas que catalizan diversos tipos de isomerización, sea óptica, geométrica, funcional, de posición, etc. Se dividen en varias subclases.
Las racemasas y las epimerasas actúan en la racemización de los aminoácidos y en la epimerización de los azúcares. Las primeras son en realidad pares de enzimas específicas para los dos isómeros y que producen un solo producto común. Las isomerasas cis – trans modifican la configuración geométrica a nivel de un doble ligadura. Las óxido – reductasas intramoleculares cetalizan la interconversión de aldosas y cetosas, oxidando un grupo CHOH y reduciendo al mismo tiempo al C = O vecino, como en el caso de la triosa fosfato isomerasa, presente en el proceso de la glucólisis ; en otros casos cambian de lugar dobles ligaduras, como en la (tabla) isopentenil fosfato isomerasa, indispensable en el cambio biosinético del escualeno y el colesterol. Por fin las transferasas intramoleculares (o mutasas) pueden facilitar el traspaso de grupos acilo, o fosforilo de una parte a otra de la molécula, como la lisolecitina acil mutasa que transforma la 2 – lisolecitina en 3 – lisolecitina, etc. Algunas isomerasa actúan realizando inversiones muy complejas, como transformar compuestos aldehídos en compuestos cetona, o viceversa. Estas ultimas desarrollan una oxidorreducción dentro de la propia molécula (oxido rreductasa intramoleculares)sobre la que actúan, quitando hidrógeno, a algunos grupos y reduciendo otros; actúan ampliamente sobre los aminoácidos, los hidroxácidos, hidratos de carbono y sus derivados.
5.Las Liasas: Estas enzimas escinden (raramente construyen) enlaces entre átomos de carbono, o bien entre carbono y oxigeno, carbono y nitrógeno, y carbono y azufre. Los grupos separados de las moléculas que de sustrato son casi el agua, el anhídrido carbónico, y el amoniaco. Algunas liasa actúan sobre compuestos orgánicos fosforados muy tóxicos, escindiéndolos; otros separan el carbono de numerosos sustratos.
6.Las Ligasas: Es un grupo de enzimas que permite la unión de dos moléculas, lo cual sucede simultáneamente a la degradación del ATP, que, en rigor, libera la energía necesaria para llevar a cabo la unión de las primeras. Se trata de un grupo de enzimas muy importantes y recién conocidas, pues antes se pensaba que este efecto se llevaba a cabo por la acción conjunta de dos enzimas, una fosfocinasa, para fosforilar a una sustancia A (A + ATP A - ℗ + ADP) y una transferasa que pasaría y uniría esa sustancia A, con otra, B (A -℗ + B A – B + Pi ). A este grupo pertenecen enzimas de gran relevancia reciente, como las aminoácido –ARNt ligasas conocidas habitualmente con el nombre de sintetasas de aminoácidos –ARNt o enzimas activadoras de aminoácidos que representan el primer paso en el proceso biosintético de las proteínas, y que forman uniones C-O; las ácido-tiol ligasas, un ejemplo típico de las cuales es la acetil coenzima. A sintetasa, que forma acetil coenzima. A partir de ácido acético y coenzima A ; las ligasas ácido – amoniaco (glutamina sintetasa), y las ligasas ácido-aminoácido o sintetasas de péptidos, algunos de cuyos ejemplos más conocidos son la glutación sintetasa, la carnosina sintetasa, etc.
La acción de estas enzimas se manifiesta con la formación de enlaces entre átomos de carbono y oxigeno de diversas moléculas, o bien entre carbono y azufre, carbono y nitrógeno y carbono y carbono. Las ligasas utilizan siempre, para el proceso de reacción, la energía proporcionada por el ATP o compuestos homólogos que son degradados, Por consiguiente las enzimas de esta clase son los únicos que intervienen en reacción no espontánea desde un punto de vista termodinámico; Actúan sobre los sustratos más diversos y revisten particular importancia en el metabolismo de los ácidos nucleicos.
Estas reacciones enzimáticas se desarrollan en dos tiempos: en el primero se forma un complejo intermedio con potencia energética muy alta-, en el segundo utilizan la energía obtenida para realizar la reacción de síntesis.
|
Grupo |
Accion |
ejemplos |
|
1. Oxidoreductasas |
Catalizan reacciones de oxidorreducción.
Tras la acción catálica quedan modificados en
su grado de oxidación por lo que debe ser
transformados antes de volver a actuar de nuevo. |
Dehidrogenasas Aminooxidasa Deaminasas Catalasas |
|
2. Transferasas |
Transfieren grupos activos
(obtenidos de la ruptura de ciertas moléculas)a
otras sustancias receptoras. Suelen actuar en procesos de
interconversiones de azucares, de aminoácidos,
etc |
Transaldolasas Transcetolasas Transaminasas |
|
3. Hidrolasas |
Verifican reacciones de hidrólisis con la
consiguiente obtención de monómeros a partir
de polímeros. Suele ser de tipo digestivo, por lo
que normalmente actúan en primer lugar |
Glucosidasas Lipasas Peptidasas Esterasas Fosfatasas |
|
4. Isomerasas |
Actúan sobre determinadas moléculas
obteniendo de ellas sus isómeros de función o
de posición. Suelen actuar en procesos de
interconversion |
Isomerasas de azúcar Epimerasas Mutasas |
|
5. Liasas |
Realizan la degradación o síntesis
(entonces se llaman sintetasas) de los enlaces denominados
fuertes sin ir acoplados a sustancias de alto valor
energético. |
Aldolasas Decarboxilasas |
|
6. Ligasas |
Realizan la degradación o síntesis
de los enlaces fuertes mediante el acoplamiento a
sustancias ricas en energía como los nucleosidos del
ATP |
Carboxilasas Peptidosintetasas |
Los sistemas enzimáticos en general, están formados por la enzima propiamente dicha (apoenzima), el sustrato o los sustratos un grupo proteico ( o coenzimas) y sustancias activadoras. La estructura formada por la apoenzima y la coenzima se denomina boloenzima; con cierta frecuencia se reconocen sistemas enzimaticos que no tienen grupo prostético o activadores reconocidos.
Apoenzima: concepto del centro activo
La apoenzima es la enzima propiamente dicha, de naturaleza proteica formada por cadenas de polipéptidos, con peso moléculas elevado, no dializable y termolábil.
Las estudiadas analíticamente hasta ahora, han sido, por razones técnicas de peso molecular bajo, 12 a 24 000, tienen una sola cadena polipeptídica (ribonucleasa, papaina, tripsina, pepcina, etc.) excepto uno o dos casos (a - quimotripsina y aldolasa) que tienen dos.
El análisis de los aminoácidos que componen a diversas enzimas demuestran que tienen una estructura similar a la de cualquier proteína; existen, de hecho unos cuantos casos en los que se ha determinado su secuencia completa, es decir, el orden en el que están dispuestos todos ellos en la cadena. El análisis de la estructura secundaria de la proteína, osea el modo como la cadena peptídoica se dispone a lo largo de su eje mayor y el de la estructura terciaria, osea la forma en que la cadena se pliega y se acomoda para formar una estructura tridimensional se conocen muy mal para todas las enzimas. Solo en el caso de la lisozima (enzima presente en las lágrimas donde funciona como un antiséptico suave y que tiene la capacidad de atacar a los polisacáridos que forman la pared de diversas bactérias) se ha determinado la estructura tridimensional de una enzima; para este fin se aplican las técnicas de cristalografía de rayos x, con una solución de dos Å, lo que demostró que la lisosima es una proteína con su cadena de 129 aminoácidos ampliamente plegada y en la que se reconoce una hendidura representante del centro activo donde se acomodan muy bien los inhibidores – ciertos compuestos del tipo de carbohidratos – que nulifican su actividad enzimática. Se ha demostrado, en este caso, que es cierta regla general de que el modo como se ordenan y disponen los aminoácidos de termoina el arreglo espacial que permite a las otras partes del sistema enzimático – sustratos, cofactores, iones, etc. – adaptarse, en el espacio, en forma adecuada, para que se lleve a cabo la acción catalítica. Por lo tanto, las estructuras indispensables que permiten la combinación con el sustrato y que confieren propiedades enzimáticas a la molécula se denomina "centro activo". Se acepta que el centro activo no es una parte muy grande de la enzima completa y, en ciertos sistemas estudiados por medio de bloqueos químicos no parece constituir una zona de más de 20 Å de diámetro. Es muy posible que el centro activo esté formado por la contribución de grupos funcionales de aminoácidos situados en distintas cadenas o en diferentes repliegues de una cadena, asiendo aparecer a dichos grupos muy distantes entre ellos si se considera el orden que guardan a lo largo de la cadena polipeptídica.
Un caso muy ilustrativo sobre lo que significa la estructura del centro activo desde el punto de vista de la composición de los aminoácidos es el de la triptofano pirrolasa, enzima ampliamente estudiada en bacterias desde el punto de vista de la bioquímica genética. En ella, la modificación de algunos aminoácidos produce perdida e la actividad enzimática, que se recupera si vuelve a incluirse los aminoácidos en el orden original; sin embargo, se pueden reemplazar dos de ellos por otros completamente distintos, y la enzima vuelve a ser totalmente activa. Es posible que con estos nuevos aminoácidos se consigan también las condiciones de distribución espacial de grupos funcionales y estructuras necesarias para la actividad enzimática.
El concepto de arreglo tridimensional adecuado de los aminoácidos que forman la cadena polipeptídica de la enzima para lograr la actividad funcional correcta permite entender numerosos denómenos: la necesidad de que la molécula proteica íntegra esté preservada en su forma; el hecho de que la desnaturalización de la enzima al permitir la separación de los pliegues, conduce a la perdida de la actividad enzimática; que al calentar una enzima con su sustrato (por ejemplo, la invertasa con sacaroza, la transaminasa con ácido a -cetoglutárico), se impide una desnaturalización que sin ellos se produciría, pues es posible que el propio sustrato contribuya a sostener y reforzar la aproximación de los pliegues de la cadena, etc.
También se entiende por que al atacar la ribonucleasa con pepsina y romper una sola unión peptídica que separa un tetrapéptido del extremo con grupo carboxilo libre se pierde la actividad, mientras que si solo se quita los tres últimos disminuye su acción sugiriendo así la importancia del residuo de ácido aspártico para sostener el centro activo en condiciones de eficiencia, o lo que es más probable, para formar parte del propio centro activo. Si se parte la ribonucleasa entre los aminoácidos 20 y 21, y se separan los dos fragmentos, ninguno es activo, pero basta mezclarlos para que se unan en tal forma que se restablece la actividad, aunque un poco menor que la originalmente observada.
El estudio detallado de la estructura del centro activo se hace por medio de inhibidores o de reactivos que se combinan de modo específico, con algunos de los aminoácidos del centro activo tales como el diisopropilfluorofosfato (DFP), que se combina con el OH del aminoácido serina, en diversas esterasas, peptidasas, etc. , e inactiva el centro activo del que forman parte dicho aminoácido; este inhibidor, aún a concentraciones de 10-10 M, inhibe a la acetilcolinesterasa; mucho de los derivados del DFP se utilizan como gases de guerra o como insecticidas (parathion), y su utilidad se debe, en rigor a su capacidad para destruir funcionalmente ciertas enzimas.
La unión del DFP al aminoácido cedina es muy estrecha y a permitido el análisis de los aminoácidos vecinos a él, haciendo un estudio de su ordenamiento en el centro activo. La secuencia de los centros activos de diversas enzimas hidrolíticas sensibles al DFP, se demuestran que la mayoría tienen cerina y a demás un aminoácido dicarboxílico (aspártico o glutámico) y en el otro un aminoácido neutro (alanina o glicina). También se ha demostrado que la histidina, cuando menos para el caso de la quimotripsina, forma parte del centro activo aún cuando el análisis de la secuencia no demuestra que exista cerca de la cerina ninguna histidina; se trata, por lo tanto, de otro ejemplo de una aminoácido, alejado e otro, y en distinto pliegue de la cadena, que integra el centro activo.
Teniendo en cuenta estos hechos, se deduce, por lo tanto, que la actividad de la enzima depende en parte de la disposición o arreglos de los aminoácidos y grupos prostéticos en determinada región de la proteína. Los aminoácidos que componen a las proteínas pueden tener moderadas actividades catalíticas, aunque de ninguna manera comparable en su magnitud, cuando se les considera en forma aislada, a las que muestran la gran molécula proteica. De hecho para muchos sistemas enzimáticos se han ideado modelos análogos, osea sustancias químicas sencillas que suelen reproducir los efectos ocasionados por la enzima, tal es el caso de los análogos, a base de piridoxsal que representan la parte activa de enzimas descarboxilantes y transaminantes. Esto no significa que necesariamente, en el estado natural, la enzima funcione como lo hace el análogo pues muchos sistemas pudieran tener otro mecanismo de operación; la hidrólisis del almidón lo mismo se logra con la adición del ácido que con la enzima específica amilasa, aún cuando en el primer caso se atacan indiscriminadamente numerosas uniones glucosídicas, y con la enzima, en cambio solo se desprenden, uno tras otro fragmentos de dos unidades de glucosa de los extremos de las ramificaciones.
- Conformación de la enzima y propiedades del centro activo. La propiedad catalítica de las enzimas parece depender de la facilidad con la que ayudan a que se pongan en contacto las sustancias reaccionantes para dar el producto o los productos de la reacción. Esto implica que el sistema enzimático tenga una conformación especial osea, una disposición adecuada de os grupos funcionales – aminoácidos de la apoenzima y grupos prostéticos, cuando existen estos – y de las moléculas mismas de los sustratos que se unirán a aquellos y permitirán que se lleve a cabo la reacción química. Este acercamiento de las sustancias reaccionantes de los grupos prostéticos y los grupos funcionales fue las razón del modelo de Ehrlich, conocido clásicamente como de la "llave y la cerradura". Así la enzima sería un molde tridimensional en negativo, de la estructura también tridimensional, en positivo de los reaccionantes que se adaptarían perfectamente a ala disposición de la enzima. Sin embargo ha sido necesario reconsiderar esta situación y sugerir – de acuerdo con Koshland – la teoría de un "acomodo inducido".
Se ejemplifican estas ideas en A se encuentra la enzima en una forma desplegada con ciertos grupos reactivos (+) y (-), colocados en una zona de la superficie de la enzima. La entrada de un cofactor F1, modifica una parte del sistema (B); se introduce en el sistema un nuevo arreglo a base de la reactividad de tipo electrónico entre la zona (+) y una parte del cofactor F1, recién introducido; por fin la entrada de un nuevo reaccionate F2 modifica la parte terminal de la enzima de manera que permite la entrada del otro reaccionante (sustrato) que se acomoda en un lugar preparado previamente por los reaccionantes F1 y F2, y permite de esta manera echar a andar la reacción catalítica. Los cambios conformacionales, se pueden demostrar con diversos métodos algunos de tipo físico, como son las modificaciones en la rotación óptica o en el patrón de sedimentación en el campo gravitacional de la ultracentrífuga, o químicos como el aumento o la disminución de la actividad enzimática bajo la influencia de cambios térmicos o la adición de agentes desnaturalizantes. Basten unos cuantos ejemplos: la transaminasa a -cetoglutárica se pude calentar a 65° C. en presencia de su sustrato sin que se afecte, al paso que la enzima sola es rápidamente degradada, cambia de configuración y se precipita; la miosina, proteína muscular contráctil, en presencia de ATP hace más notable su forma de espiral y permite el reconocimiento de aminoácidos previamente ocultos en sus pliegues; la D-amino oxidasa, al unirse a su cofactor, el FAD, pasa de la forma espiral en a -hélice, a una disposición irregular distribuida al azar.




No hay comentarios.:
Publicar un comentario